歐美發達國家通過完善的知識產權保護、良好的市場機制和嚴格的準入條件構筑了較高的市場壁壘,通常我們稱之為規范市場。由于競爭壁壘較高直接導致規范市場的藥品價格遠高于中國為代表的非規范市場。以歐美發達國家為代表的醫藥市場價值占世界醫藥市場份額的80%以上。相比之下國內化學制劑業的銷售收入不到發達國家醫藥市場價值的1/30。一批重磅炸彈級的專利藥品逐漸結束保護期,專利藥品的市場迅速擴大,仿制藥的市場價值已經遠高于原料藥。另一方面,迫于不斷高漲的醫療支出,歐美發達國家大力推行仿制藥替代原研藥的計劃也促進了仿制藥市場的增長。
由于近年來一系列鼓勵仿制藥替代政策的出臺,預計將使中國的仿制藥市場份額由現在的38%上升到60%,而過期原研藥的份額則由目前的55%下降到20%。一致性評價是很好的決策,但時間短,企業壓力很大。美國、歐洲、日本市場,一致性評價經歷了10-15年,中國給的時間比較短,但這是利國利民的好事。
名詞解釋:仿制藥質量和療效一致性評價是指對已經批準上市的仿制藥,按與原研藥品質量和療效一致的原則,分期分批進行質量一致性評價,使仿制藥在質量與藥效上達到與原研藥一致的水平。
根據原國家食藥監總局公布的《2018年底前須完成仿制藥一致性評價品種目錄》(以下簡稱“289目錄”)要求,289種仿制藥在2018年底前要完成一致性評價,涉及17740個批準文號,1800多家企業。據不完全統計,僅有34個品種出現了通過一致性評價的產品,涉及30家企業的66個批準文號。其中屬于289目錄內的共有17個品種,“過關”產品比率僅為5.88%。
政府要想讓市場上流通的藥品質量好價格又合理,唯有打開中國市場,進行全球化采購,倒逼藥企提升研發能力的同時,也能讓更多“價廉物美”的藥品進入中國市場,讓老百姓得到實惠。
根據海關統計口徑:目前海關系統針對藥品制劑產品的進出口貿易統計,納入下列專項統計:3003兩種或兩種以上成分混合而成的治病或防病藥品(不包括品目3002/3005或3006的貨品),未配定劑量或制成零售包裝;3004由混合或非混合產品構成的治病或防病用藥品(不包括品目3002/3005或3006的貨品),已配定劑量(包括制成皮膚攝入形式的)或制成零售包裝。根據中國海關數據顯示,近年我國混合或非混合產品構成的治病或防病用藥品進出口數量及金額呈波動趨勢,2017我國混合或非混合產品構成的治病或防病用藥品出口量達到36.3萬噸、出口額達到36.6億美元、進口量達到9.5萬噸、進口額達到174.3億美元。2011-2017年我國混合或非混合產品構成的治病或防病用藥品進出口數量及金額分析如下:
2011-2017年中國混合或非混合產品構成的治病或防病用藥品出口數量
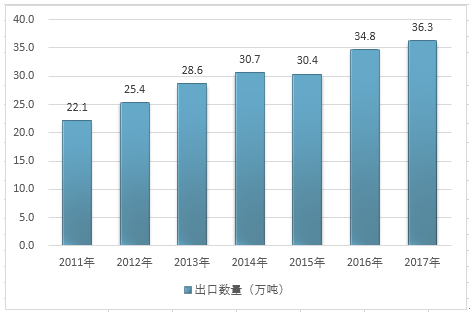
資料來源:中國海關、智研咨詢整理
2011-2017年中國混合或非混合產品構成的治病或防病用藥品出口金額
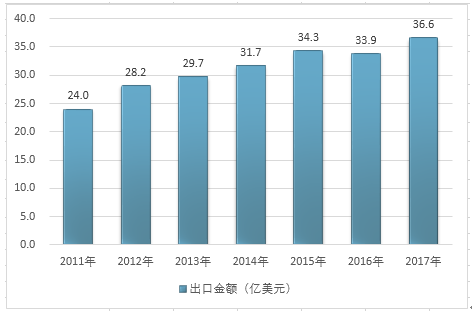
資料來源:中國海關、智研咨詢整理
2011-2017年中國混合或非混合產品構成的治病或防病用藥品進口數量
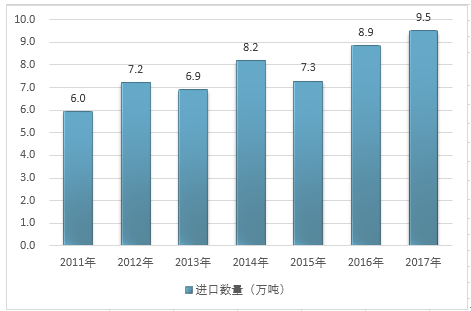
資料來源:中國海關、智研咨詢整理
2011-2017年中國混合或非混合產品構成的治病或防病用藥品進口金額
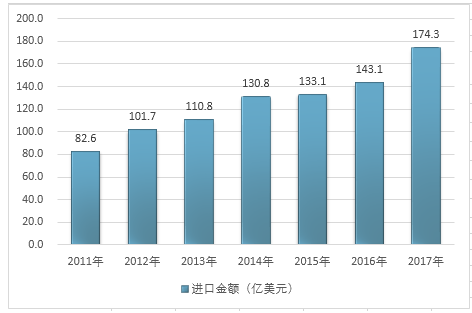
資料來源:中國海關、智研咨詢整理
歐美發達國家的有完善的法律和行政體系對藥品的安全作出了詳細的規定,其市場準入不僅僅包括了制劑生產線的認證還包括諸如原料藥、環保等多種軟件和硬件。目前,雖然有近50家制劑企業通過了歐、美、日相關認證,但主要是針對特定的產品線,尤以片劑和粉針為主,產品本身在國外的競爭力并不一定強。實際上,國內一些企業做高端認證并不是為了拓展海外市場,而是為了能夠在國內藥品招標中進入更高的質量層次。中國藥企要想成功拓展海外市場,不但需要提高產品質量、加快認證步伐,而且還應加大對重點市場的分析,做好到期專利品種的篩選和渠道建設,真正融入當地市場運行體系和醫療體系。
隨著國際化路徑的多元化,不少企業開始在國外成立子公司或合資公司,從事創新藥物的研發和注冊支持,取得了一定的進展。但也有不少企業的境外投資項目處于停滯狀態,這就需要企業根據自身情況,對目標市場的投資環境和市場前景進行認真調研,選擇適銷對路的產品進行開發。而對于一些中小企業來說,融資渠道少,銀行融資受到擔保、自身規模等的限制,因此可引入外部資本,這樣企業在境外投資設廠以及合資過程中,既能獲得信譽認可,也可降低融資擔保風險。

 公眾號
公眾號
 小程序
小程序
 微信咨詢
微信咨詢
























